今日上午,国家药监局正式发布《关于优化创新药临床试验审评审批有关事项的公告》,其中提到:为进一步支持以临床价值为导向的创新药研发,提高临床研发质效,对符合要求的创新药临床试验申请,在受理后30个工作日内完成审评审批。
此外,上述单位同步发布了政策解读稿。关于“为什么要在药物临床试验60日默示许可基础上增加30日通道?”,其表示,我国临床研发资源丰富,近年来我国药物临床试验机构和专业人员的经验、能力不断提升,早期、深入参与全球研发创新的条件已趋成熟。为此,国家药监局统筹现有审评审批资源,对部分有进一步加速需求的临床试验申请再提速。
解读稿进一步指出,国家药监局支持符合条件的全球同步研发品种和国际多中心临床试验纳入30日通道。I期、II期临床试验是早期探索性临床试验,全球同步研发既可在我国单独进行,也可在不同国家进行。我国主要研究者早期参与临床研发,有助于创新药全球同步研发更加适应中国临床实践,更好服务我国患者。
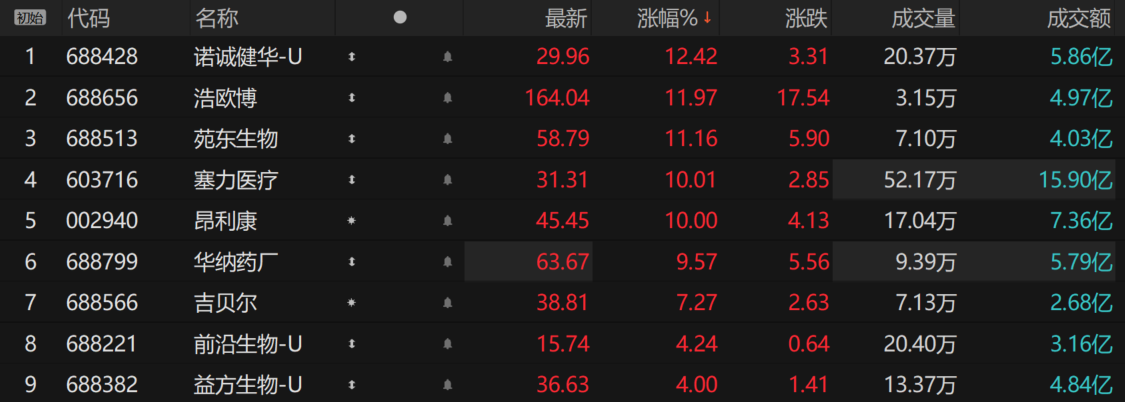
受上述消息影响,午后创新药概念再度发力。截至发稿,塞力医疗涨停,诺诚健华涨超12%,华纳药厂、苑东生物涨超10%,益方生物、前沿生物等跟涨。
近年来,我国创新药研发能力显著增强。据记者统计,今年来已有64款药物被国家药监局药审中心(CDE)正式纳入突破性治疗品种名单。2022-2024年的进入突破性治疗品种名单的药物数量为56款、69款、94款。
与此同时,创新药板块收入迎来强劲增长。据招银国际统计,2025年上半年A股和港股上市的393家医药公司中,创新药板块表现最佳,收入平均增长35%,维持强劲势头,主要由于创新药享受较为积极的医保支付环境,以及多家创新药企业实现了品种出海授权。多家创新药企业大幅减亏乃至实现经营利润转正。
值得一提的是,日前“美国方面或对中国创新药设限”的市场传闻,一度对二级市场产生影响。海通国际认为,以行政命令的形式限制来自中国的药品,其最终落地的可能性仍然有较大的不确定性。在实操过程中,行政命令的稳定性和效力远远低于法案,且具有司法挑战、利益集团游说、执行难度大等特点。
该机构进一步表示,中国药企产品质量不断提升,具备全球竞争力,短期内医药板块表现受情绪影响,波动可能加剧。但中国目前开展的临床试验数量快速提升,中国药企产品质量不断提升,具备全球竞争力,长期工程师红利不改变,看好中国制药企业长期向全球输出Best-in-class品种。
本文版权归原作者所有,择尔裕【智慧+】APP仅为传播更多有价值的信息,若您发现文章内容有版权问题,请把相关链接提交至邮箱:mssj@ytfjr.com,我们将及时进行处理。文章内容不构成投资建议,市场有风险,投资需谨慎!




